可穿戴的tFUS工程化关键路在何方?
经颅低强度聚焦超声(LIFU)是一种新兴的非侵入性神经调控技术,具有毫米级空间分辨率和深部靶点可达性,有望用于治疗抑郁症等精神疾病。然而,现有tFUS系统要么依赖全程MRI引导、体积庞大(如ExAblate Neuro),要么采用单阵元机械扫描、无法电子转向,且缺乏穿戴性,限制了重复治疗的应用。因此,设计一套可穿戴、可电子转向、无需医院基础设施的LIFU系统成为迫切需求。
本系统设计的三个关键理念为:
头戴式轻量化结构:将换能器集成于3D打印头架,总重仅2.5磅,确保长时间佩戴的舒适性与稳定性。
电子波束成形:采用128阵元二维矩阵阵列,通过控制各阵元发射延时,实现焦点在三维空间内快速、无声移动,避免机械扫描的笨重与缓慢。
分层定位策略:结合光学神经导航(粗定位)与电子转向(精定位),既降低了对操作者精度的要求,又保证了个体化靶点的可达性。
HUIYING
可穿戴系统设计详解
头架与换能器集成
系统采用定制3D打印头架,可牢固贴合于参与者前额及颅顶。头架正面留有开口,用于放置超声换能器阵列。如图1所示(图1左为换能器与外壳,右为头架安装在假人头上),头架下缘设有中央定位支撑,正好位于眉间上方,确保每次佩戴的可重复性。

图1 – 换能器外壳与头戴装置
图1左显示了安装在3D打印外壳中的换能器阵列,外壳上固定有三个反光球(用于光学导航追踪)。图1右图展示了头戴装置固定在假人头部上的照片,头架正面留有开口用于放置换能器,并可见另一组反光球用于头架本身的配准。
换能器阵列通过水平滑动机构与头架连接,可在不拆卸头架的情况下横向移动±2 cm,便于根据个体解剖调整入射位置。换能器自身带有曲率设计,与额头自然曲线匹配,配合楔形耦合垫(如图2右)使换能器向下倾斜10°,从而将超声能量导向深部前额叶靶点(如amPFC)。
图2 – 佩戴状态与楔形耦合垫
图2左为换能器通过水平滑动机构安装在头架上的完整佩戴状态。右图为特制的楔形聚合物耦合垫,其10°楔角使换能器自然向下倾斜,以适配前额解剖曲线并将超声束导向深部前额叶靶点(如amPFC)。
声耦合与温度监测
换能器与皮肤之间使用定制聚合物凝胶垫及一层薄超声凝胶,保证声能高效透入,同时避免空气间隙造成的反射损失。凝胶垫采用平面‑凸面模具制成,使其在贴合换能器曲率的同时,又能适配典型额头形状。
在换能器表面四个角落嵌有两个热敏电阻,实时监测温度。一旦温度异常,操作者可通过软件在1秒内中止超声发射,或直接摘除头架实现硬件级紧急停止。
佩戴舒适性与可接受性
在20名健康志愿者的研究中,所有参与者均完成了10分钟连续佩戴与超声递送。主观感受问卷显示,多数不良反应(如刺痛、振动)的中位数评分为0–2(10分制),且无一人因不适提前中止。部分参与者甚至报告“感觉放松”。这表明该头戴装置具有良好的耐受性。
HUIYING
可转向系统设计详解
电子转向原理与范围
系统使用128阵元二维矩阵阵列(如图3),每个阵元可独立控制发射延时。通过调整各阵元的相对延时,可使超声束在空间内聚焦并移动,这一过程无需机械运动,因此称为“电子转向”。

图3 – 定制曲面矩阵超声换能器
图3中展示了本系统核心的定制400 kHz二维矩阵换能器,具有11行×12列阵元(四角未连接),阵元间距4.1 mm,水平方向曲率半径50 mm。换能器后部连接2米长屏蔽线缆及260针ZIF连接器,表面可见用于温度监测的热敏电阻位置。
经水槽实验标定(与仿真结果误差<5%),该阵列的名义转向范围为:侧向(x)±12.5 mm,仰角(y)−20~+10 mm,轴向(z)40~60 mm(坐标原点位于阵列几何中心前方50 mm处)。但考虑到热安全(颅骨热指数TIC<3)及栅瓣抑制(次级波瓣压力不超过主瓣50%),实际安全转向体积缩小为:侧向1.8 cm、仰角2.5 cm、轴向2 cm,中心位于皮肤下5 cm处。
双模式定位:机械滑动 + 电子转向
仅靠电子转向无法覆盖整个前额叶区域,因此系统设计了机械滑动 + 电子转向的双模式定位:
机械滑动:换能器可在头架上横向移动±2 cm,将整个电子转向体积平移至不同横向区间。
电子转向:在每个机械位置上,电子转向在1.8 cm×2.5 cm×2 cm范围内精细调整焦点。
二者叠加后,系统可覆盖侧向约6.5 cm、深度40–60 mm的连续区域,足以抵达大部分前额叶皮层靶点(如背外侧、腹内侧、前扣带回等)。图4显示了20名参与者的个体化靶点在安全转向体积内的分布,全部位于TIC<2.5的安全区域。
图4 – 基于TIC的安全转向体积
图4背景色阶图显示了在阶段1.3最激进参数(PNP=820 kPa)下,不同转向位置对应的颅骨热指数(TIC)。白色圆圈标记了20名参与者实际靶点在转向体积内的分布。所有靶点均位于TIC<2.5的区域(远低于安全限值3.0),表明系统能在足够大的范围内安全转向。
虚拟配准:个体化避开鼻窦
在研究中发现,部分参与者的额窦或筛窦会遮挡超声路径。为此,团队事后开发了“虚拟配准”算法:利用MRI数据,对121个候选换能器放置位置逐一模拟从每个阵元到靶点的声线,检测是否经过窦腔(空气会完全阻挡超声)。然后选出既能满足转向范围要求、又使被遮挡阵元数最少的优化位置。如图5所示,绿色点为无遮挡的入射点,红色点为被窦腔阻挡的点,黄色半透明为分割出的窦腔。
图5中黄色半透明区域为分割出的鼻窦腔,青色圆点为靶点,绿色点为无阻塞的阵元入射点,红色点为被窦腔阻挡的入射点。通过该可视化,操作者可选择最优换能器放置位置(尽可能多绿色点)。图5展示了虚拟配准算法的输出,用于前瞻性指导探头摆放。
应用该虚拟配准后,19名可分析参与者中,仅1人因窦腔过大导致>30%阵元无法避免遮挡,其余均可通过优化放置实现无遮挡或<20%遮挡。该技术将集成到未来研究中,进一步提高递送效率。
HUIYING
经颅低强度聚焦超声系统硬件详解
系统总体框架
整套系统包含四大硬件/软件组件(如图6框图):
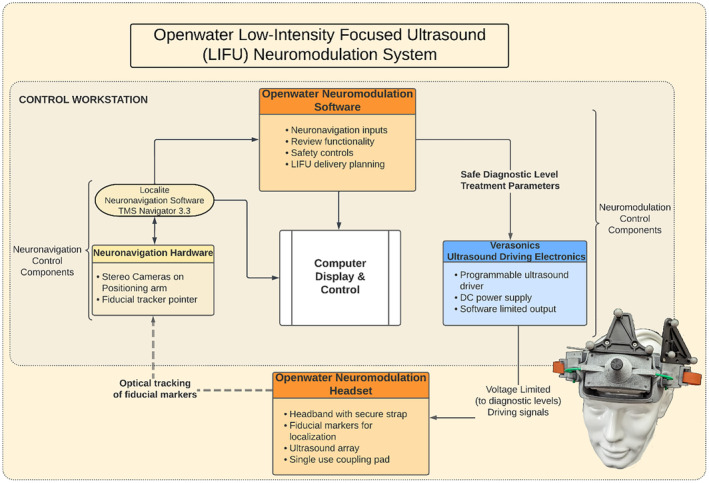
图6 – 系统组件框图
图6展示了Openwater低强度聚焦超声神经调控系统的四大核心组件:可穿戴头戴设备(含超声矩阵阵列)、光学神经导航系统(用于配准MRI与换能器)、神经调控规划软件(用于波束成形与仿真)以及超声驱动电子设备(Verasonics平台)。图6中清晰标明了各组件之间的数据与控制流向,为理解系统整体架构提供了顶层视图。
可穿戴头戴装置(含换能器、头架、耦合垫)
光学神经导航系统(Localite,含立体相机及反光球)
超声驱动电子系统(Verasonics Vantage平台)
控制与规划软件(MATLAB开发)
图7展示了实际设备照片:移动推车上放置了计算机、驱动电子机箱、直流电源、换能器连接器,以及用于神经导航的立体相机(安装在可升降立柱上)。

图7 – 系统硬件实物照片
图7显示了安装在移动推车上的完整系统硬件,包括显示器、计算机主机、Verasonics驱动电子机箱、直流电源、换能器连接接口以及用于神经导航的立体相机(安装在可升降立柱上)。图2 直观呈现了系统的实际物理布局,展示了其便携性与集成度。
超声换能器阵列
类型:二维矩阵阵列,11行×12列,但四个角上的阵元未连接,实际使用128个有效阵元。
中心频率:400 kHz。
几何聚焦:水平方向具有50 mm曲率半径的圆柱面聚焦,垂直方向无几何聚焦(依赖电子转向)。
阵元尺寸:方形,边长4.1 mm(间距),总面积约21.5 cm²。
匹配网络:在换能器PCB上为每个阵元串联电感,以抵消400 kHz时的容性阻抗,提高功率传输效率。
连接:通过2米长屏蔽线缆及260针Cannon ZIF连接器接至驱动电子系统。
驱动电子系统:Verasonics Vantage平台
Verasonics Vantage 128 HIFU版是系统的发射与控制核心,其关键特性如下:
| 特性 | 规格 |
| 通道数 | 128 发射/接收 |
| 输出电压 | 2~190 Vpp(峰峰值) |
| 延时精度 | 4纳秒(250 MHz时钟) |
| 波形 | 三电平双极性方波 |
| 外部电源 | 1200 W DC电源(两路并联) |
| 软件接口 | MATLAB + C/C++ MEX |
发射路径:每通道独立可编程脉冲发生器,支持延时(4 ns步长)、脉冲宽度、极性、切趾等参数。HIFU选项允许毫秒级长脉冲(脉冲长度50–100 ms),且通过外置大功率电源实现高达820 kPa的峰值负压。
接收与监测:虽然本研究主要使用发射功能,但Vantage也支持14位、62.5 MHz采样率的回波采集,为未来像差校正或温度监测提供可能。换能器上的热敏电阻通过辅助通道接入,实时反馈温度。
软件控制:MATLAB脚本负责波束成形计算(基于k‑wave仿真,如图8。软件界面主要分为左右两大区域:左侧区域:显示参与者的MRI解剖图像,并在此基础上叠加换能器模型、靶点标记、模拟声场(压力或强度等值线)。该区域用于可视化验证换能器与靶点的空间关系,以及超声束的预期分布。右侧区域:是一个多标签或可滚动的控制面板(Plan Panel),包含治疗协议的参数设置、当前解决方案的统计分析(如峰值负压、机械指数、热指数、束宽等),以及启动/中止超声递送的控件)、安全参数校验(MI、TIC、ISPTA)、电压缩放及时序配置。计算出的延时和电压通过PCIe总线下载至硬件定序器,然后独立运行,保证实时性。
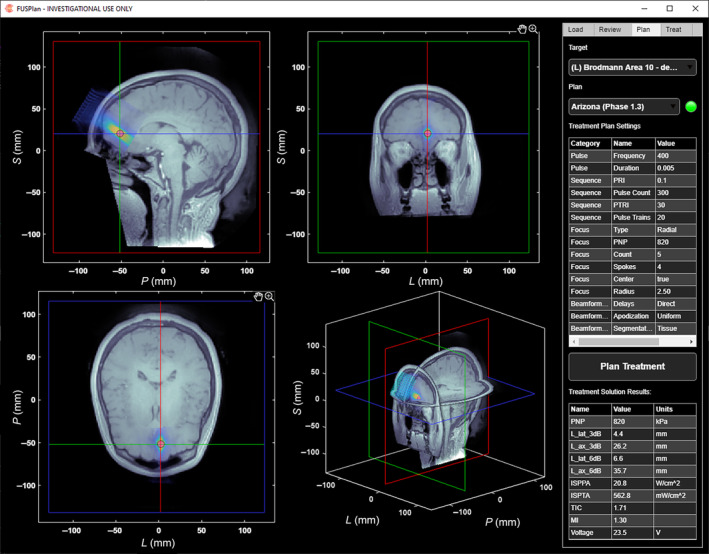
图8 规划软件截图
图8所展示的规划软件界面分为左右两区:左侧显示参与者的MRI三视图,并叠加换能器模型、靶点标记以及模拟声场的等值线(-3 dB、-6 dB等);右侧为控制面板,包含治疗参数设置(频率、脉冲长度、目标压力等)、波束成形选项、仿真结果(PNP、MI、TIC、束宽)以及启动/中止控件。该界面是操作者进行个体化规划与监控的中枢。
神经导航与配准
Localite光学导航系统通过立体相机追踪头架和换能器上的反光球(换能器上有三个已知几何关系的反光球,头架上另有一组)。相机精度为0.35 mm RMS。操作流程如下:
获取参与者的T1及PETRA MRI(用于分割颅骨和窦腔)。
在Localite软件中将MRI与参与者头部解剖标志(鼻尖、耳屏等)配准。
将换能器注册到导航系统中(通过专用校准工具)。
操作者将换能器大致放置在额头,软件实时计算当前转向需求及被遮挡阵元数。
这一流程使得粗定位只需“大致瞄准”,因为后续电子转向可补偿数毫米的偏差。
HUIYING
临床研究
研究方法
参与者:20名健康右利手成年人(16女,4男),平均年龄23.6岁。入组标准包括有一定程度的重复性负性思维(PTQ评分高于25百分位),但排除任何精神或神经疾病史、头部金属植入物、MRI禁忌症等。
靶点:左侧前内侧前额叶皮层(amPFC,MNI坐标约−5,45,−35 mm),该区域是默认模式网络的核心节点,与自我参照思维及抑郁症的过度连接有关。
超声参数:采用阶梯式递增方案以确保安全:
阶段1.1(9人):单焦点,PNP=510 kPa,ISPTA=201 mW/cm²,MI=0.8。
阶段1.2(6人):多焦点(径向五点交叠脉冲,如图9C、9D),PNP=650 kPa,ISPTA=327 mW/cm²,MI=1.03。
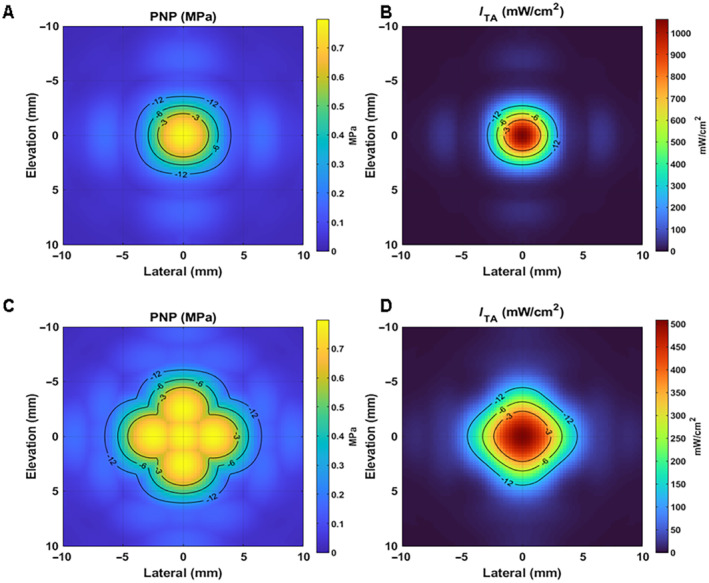
图9 – 单焦点与多焦点声场模式
图9A、图9B为单焦点模式在侧向-仰角平面上的压力场(A)和强度场(B)等值线图(-12、-6、-3 dB),显示典型“雪茄形”焦斑。图9C、D为阶段1.2和1.3中使用的径向五点交叠多焦点模式,五个焦点呈十字形分布,间距5 mm,用以扩大有效调控区域而不增加单点ISPTA。
阶段1.3(5人):同上多焦点,PNP=820 kPa,ISPTA=508 mW/cm²,MI=1.3。
所有阶段均采用脉冲串:脉冲宽度50 ms,脉冲重复间隔100 ms(阶段1.1)或根据多焦点轮换调整(图10)。总超声暴露时间10分钟。
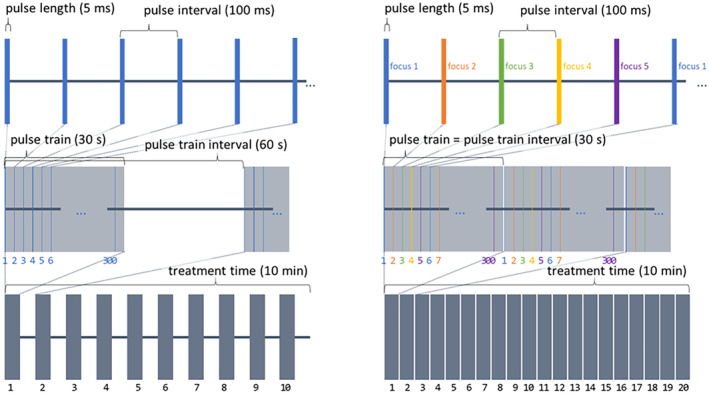
图10 – 脉冲序列对比
图10左为阶段1.1的单焦点脉冲序列:每个脉冲串持续30秒,随后30秒关闭,循环交替。图10右为阶段1.2/1.3的多焦点交叠脉冲序列:五个焦点按顺序循环发射,每个焦点脉冲长度50 ms,脉冲重复间隔延长,从而在无强制关断的情况下连续递送10分钟,实现空间平均能量分布。
安全评估:
主观:递送前后询问不适感,并采用0–10分问卷评估刺痛、发热、振动、疼痛等感觉。
影像学:递送后约30分钟行磁敏感加权成像(SWI),由两名神经放射科医生盲法读片,检测有无微出血。
生理:换能器表面温度监测。
研究结果
可穿戴性与可转向性:
所有20名参与者的amPFC均位于系统安全转向体积内(图4),侧向位置平均−0.9±2.6 mm,仰角−3.5±5.8 mm,轴向50.5±3.7 mm。
操作者报告头架佩戴简单,界面引导有效;虚拟配准事后分析显示,通过优化放置可避免大部分窦腔遮挡。
安全性:
无严重不良事件。无参与者提前退出。
SWI影像:所有20例扫描均判读为正常,未见任何微出血征象。
主观感觉:如下表所示,各项感觉的中位数均为0(无感觉),最大评分分别为:发热5分(1人)、振动/脉冲8分(但仅1人)、声音9分(但可能源于系统噪声而非不适)。疼痛最高仅2分,且归因于头架压力而非超声本身。
| 感觉 | 最大评分 | 中位数 | 均值 |
| 瘙痒 | 4 | 0 | 0.4 |
| 发热/灼烧 | 5 | 0 | 0.6 |
| 刺痛 | 8 | 0 | 2.6 |
| 振动/脉冲 | 8 | 0 | 2.1 |
| 声音 | 9 | 0 | 2.15 |
| 紧张 | 8 | 0 | 1.6 |
| 疼痛 | 2 | 0 | 0.25 |
热安全:换能器表面在10分钟运行时温度仅35–36°C(静止空气测试中20分钟才达42°C);仿真显示皮肤温升<4.2°C,颅骨表面温升<3°C(图11、12)。
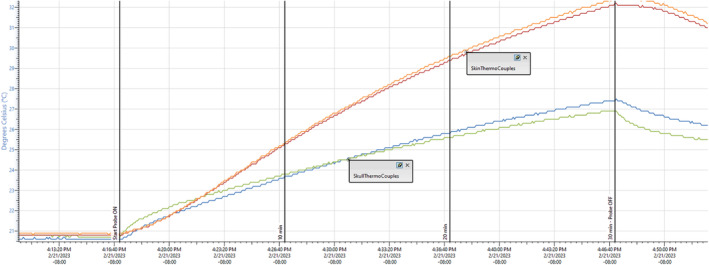
图11 – 模拟使用热测试结果
图11中蓝色和绿色曲线为仿生颅骨表面的温度变化,橙色和红色为皮肤表面的温度变化。在10分钟超声暴露结束时,皮肤表面温升约4.2°C(达25.2°C),骨表面温升低于3°C(低于24°C),均远低于组织损伤阈值,验证了系统在真实耦合条件下的热安全性。
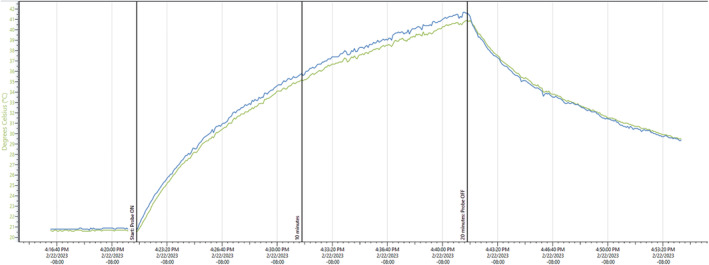
图12 – 静态空气热测试结果
图12蓝色和绿色曲线为换能器表面不同测点的温度变化。在持续20分钟发射(无耦合,无间断)后,表面温度才达到42°C;而本研究的单次最大暴露时间为10分钟,此时温度仅35–36°C。该测试证明即使误在空气中运行,也不会造成危险高温。
递送效率事后分析:
通过分割MRI并重新仿真(如图13、14),发现由于颅骨的衰减和像差,实际到达靶点的峰值负压仅为设定值的58±19%(图15)。
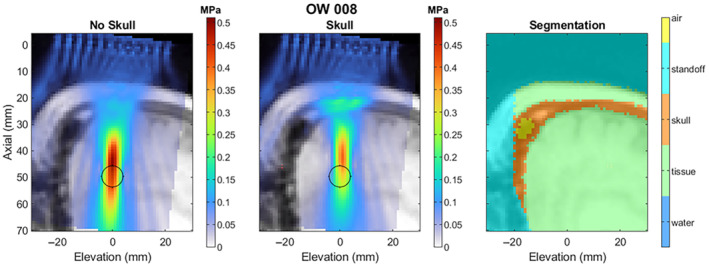
图13 – 有利颅骨几何的再仿真示例
图13中展示了某位参与者的MRI分割结果(皮肤、颅骨、脑组织)以及基于实际发射参数(含颅骨)的再仿真声场。左侧为侧向-仰角平面,右侧为轴向-侧向平面。该参与者的颅骨较薄且鼻窦较小,声束经颅后仍保持良好聚焦,焦点偏移较小。
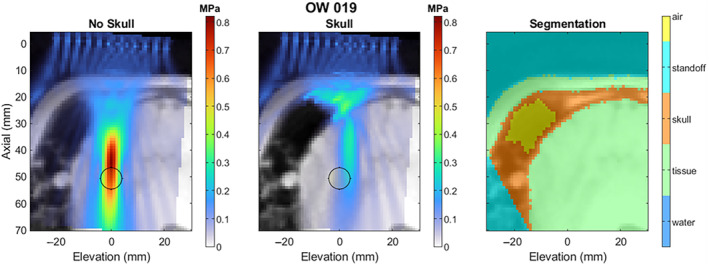
图14 – 不利颅骨几何的再仿真示例
图14参与者的额窦较大且位置居中,导致声束路径被部分遮挡。再仿真显示焦点严重畸变、峰值压力显著降低,且焦点向换能器方向偏移约10 mm。图14揭示了颅骨和窦腔个体差异对递送效率的显著影响。
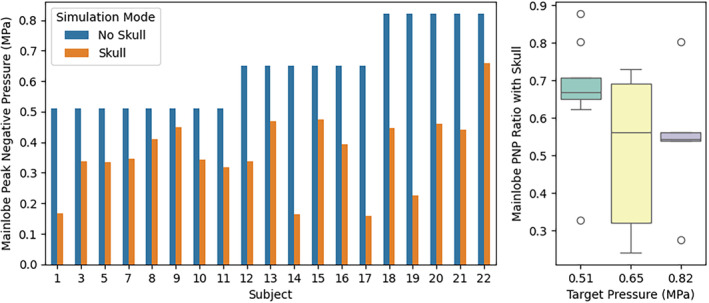
图15 – 有/无颅骨时峰值负压对比
图15比较了全部20名参与者在忽略颅骨(目标压力)与实际考虑颅骨(经颅衰减后)两种情况下模拟得到的焦点峰值负压。有颅骨时实际压力平均仅为目标值的58±19%,且个体差异大(最低仅17%)。该结果量化了颅骨衰减导致的能量损失,并强调了像差校正的必要性。
焦点位置平均向换能器方向偏移8.1±2.3 mm(轴向),但侧向偏移仅1.3±0.9 mm,仍远小于焦斑尺寸(侧向束宽约4–8 mm,轴向束宽约23–25 mm)。因此,尽管能量有损失,但靶区覆盖仍可接受。
HUIYING
总结
本研究成功设计、构建并临床验证了一套可穿戴、可电子转向的经颅低强度聚焦超声系统。其核心创新与结论如下:
可穿戴设计:3D打印头架+128阵元矩阵换能器,总重2.5磅,配合楔形耦合垫,实现了前额舒适、稳定的佩戴,10分钟递送耐受性良好。
可转向能力:通过128通道独立延时控制,实现焦点在1.8 cm×2.5 cm×2 cm体积内电子移动;结合机械滑动(±2 cm),总侧向覆盖约6.5 cm,深度40–60 mm,足以覆盖前额叶主要皮层靶点。
硬件集成:Verasonics Vantage HIFU平台提供190 Vpp、4 ns延时精度的128通道驱动,MATLAB软件实现个体化波束成形与安全校验;光学神经导航实现亚毫米级配准。
临床安全:20名健康志愿者中无不良事件,SWI无微出血,主观不适轻微,热指标远低于安全限值。阶梯式递增方案验证了最高820 kPa(PNP)的安全性。
局限与改进方向:颅骨衰减导致实际递送压力仅为目标的58%,且焦点向探头方向偏移约8 mm;部分参与者存在窦腔遮挡。未来需开发像差校正算法(通过调整各阵元延时和幅度补偿颅骨影响),并将“虚拟配准”前瞻性地用于指导探头放置,以提高递送效率和靶点精度。
综上,该系统为前额叶靶点的神经调控研究提供了安全、可穿戴、灵活转向的可靠工具,为后续在抑郁症等临床人群中的应用奠定了坚实基础。
本文 zblog模板 原创,转载保留链接!网址:https://www.wbaas.cn/fengrong/1641.html
1.本站遵循行业规范,任何转载的稿件都会明确标注作者和来源;2.本站的原创文章,请转载时务必注明文章作者和来源,不尊重原创的行为我们将追究责任;3.作者投稿可能会经我们编辑修改或补充。